
Osteosarcoma en iguana verde (Iguana iguana)
AUTOR: MVZ Ricardo Texis Guerrero
Créditos:
Laboratorio Veterinario LAPAC, Laboratorio Especialista en Patología Clínica Veterinaria, Ixtapaluca; Estado de México
Radiología Móvil Digital ADZA, Gustavo A. Madero, Ciudad de México
Resumen
El cáncer es una enfermedad que consiste en una proliferación descontrolada de células que transforman su morfología y fisiología, modificando su estructura y función. Esta enfermedad ha sido descrita por médicos, biólogos e incluso paleontólogos, lo que da testimonio de que nos ha acompañado desde que empezó la vida en la Tierra.
Anteriormente se creía que los reptiles no eran tan propensos a presentar crecimientos sugerentes de tumores, pero gracias a la investigación se ha demostrado que llegan a presentar este tipo de padecimientos de forma común e incluso característica en algunas especies.
El osteosarcoma es uno de los tumores más agresivos que se pueden desarrollar en un individuo por su alta tasa de proliferación en metástasis y por la agresividad del tratamiento, sobre todo en especies con metabolismo aletargado.
Abstract
Cancer is a disease characterized by the uncontrolled proliferation of cells that transform their morphology and physiology, thereby modifying their structure and function. This disease has been described by doctors, biologists, and even paleontologists, which testifies that it has accompanied us since life began on Earth. Previously, it was believed that reptiles were not prone to growths suggestive of tumors, but research has shown that they present this condition in a typical, even characteristic, way in some species. Osteosarcoma is one of the most aggressive tumors that can develop in an individual due to its high rate of proliferation in metastasis and the aggressiveness of the treatment, especially in species with a lethargic metabolism.
Introducción
El cáncer es una enfermedad de proliferación descontrolada de células transformadas sujetas a la evolución por selección natural con múltiples factores de predisposición.1
Todo organismo está constituido por un gran número de células, que son la unidad anatómica funcional; son entidades dinámicas con una multitud de reacciones químicas en su interior, conocidas como metabolismo celular. Contienen información hereditaria codificada en el ADN, asegurando el paso de esta información a la descendencia.2
En ocasiones, estos procesos se descontrolan por múltiples causas, lo que provoca mutaciones irreversibles que afectan el crecimiento y la división normales de las células.2 Al momento en que esto ocurre, las células no mueren por el proceso de apoptosis, sino que, por el contrario, estas nuevas células crecen y se multiplican de forma acelerada sin patrón estructural, generando una masa de tejido que es lo que denominamos tumor.3
Tumores óseos
Un tumor es un nuevo crecimiento de tejido que, aparentemente, se origina y crece de forma espontánea. Posee una arquitectura atípica, no satisface los usos del organismo y no alcanza una terminación definida de crecimiento.1
Los tumores óseos son proliferaciones anormales de células originadas dentro de un hueso, pudiendo ser malignos o benignos.4 La causa de los tumores óseos se desconoce, pero entre las posibles causas están las anomalías genéticas hereditarias, la radiación y las lesiones directas, aunque no tienen una causa específica.1
Los cánceres que comienzan en los huesos se denominan tumores óseos primarios, como el condrosarcoma, el sarcoma de Ewing, el fibrosarcoma y el osteosarcoma.4 Por otro lado, los que comienzan en otra parte se denominan tumores óseos metastásicos, que se comportan de forma diferente. Los tumores que con mayor frecuencia generan metástasis óseas son los de mama, riñón, pulmón, próstata y tiroides. A este padecimiento también se le conoce como enfermedad ósea metastásica.5
La diferencia entre los tumores primarios y los metastásicos radica en el tipo de destrucción que ocurre en la anatomía propia del hueso. El tumor primario lo que provoca es un crecimiento ralentizado propio desde la médula al exterior, causando una deformidad que puede palparse y que, al momento de realizar un estudio radiográfico, da la apariencia de una masa propia creciendo directamente en el hueso. Asimismo, provoca dolor localizado en las inmediaciones del crecimiento tumoral.5
Por su parte, el tumor metastásico causa destrucción en una zona específica, lo que provoca osteólisis. La respuesta del hueso es formar nuevos osteoblastos para intentar formar de nueva cuenta hueso, lo que puede provocar un debilitamiento y deformación.6 Esto resulta en dolor generalizado, mayor riesgo de fracturas y postración.7
Osteosarcoma
El osteosarcoma es el tumor primario en hueso más común reportado en la literatura. Representa el 85% de los tumores primarios de esqueleto y un 75% en el esqueleto apendicular.7 Aunque este tipo de tumor puede darse en cualquier porción del hueso, muestra una alta predilección por las regiones metafisarias del húmero proximal, del radio distal, el fémur distal y la tibia proximal.7,8
Ciertos factores parecen estar asociados con un peor pronóstico, como el aumento del tamaño del tumor, el alto grado y el índice mitótico,9 así como la localización anatómica. De la misma forma, la edad está asociada con una mayor mortalidad, pero no con un mayor riesgo de metástasis.10
El diagnóstico presuntivo se basa en la localización de la lesión ósea, las características dadas por los estudios de imagen (radiográfico, resonancia magnética y tomografía computarizada) y los resultados de la citología de la lesión.11
Al realizar un estudio radiográfico del sitio afectado se deben realizar dos proyecciones ortogonales de la lesión primaria (se hace énfasis en las proyecciones laterolaterales, ventrodorsales y dorsoventrales) y tres proyecciones para el estudio de metástasis pulmonar.11
Las lesiones provocadas por los osteosarcomas apendiculares son en su mayoría monostóticas, es decir, afectan a un solo hueso. Estas lesiones muestran características óseas agresivas, como la lisis cortical moteada o apolillada, con una zona de transición entre el hueso sano y el patológico, reacciones periósticas de lisas a irregulares y, en ocasiones, osteólisis y osteoproliferación.11,12
Una herramienta de gran ayuda antes de someter a un paciente a una biopsia mediante cirugía es la citología por aspiración con aguja fina. Se realiza con una aguja hipodérmica de 20G. Es una técnica rápida, no invasiva y de bajo costo que no requiere en su mayoría el uso de sedantes o tranquilizantes y, si es posible, que se puede observar directamente en la consulta.11
La precisión del diagnóstico es de entre el 70 y el 90%, derivada de la interpretación patológica de quien observa las tinciones, aunada a una técnica de tinción correcta. Las más recomendables son la tinción de Wright y la de fosfatasa alcalina.11
El diagnóstico definitivo, así como el grado de infiltración, solo puede confirmarse mediante un estudio histopatológico. Al plantear realizar un estudio, debemos considerar la biopsia, que, al realizarse en un tejido no blando, corre el riesgo de exacerbar signos y provocar fracturas durante y después del procedimiento. La mayoría de las muestras se realiza utilizando agujas Michele Trephine o aguja de Jamshidi. Se recomienda una sola muestra y, de preferencia, de la zona central del periostio para observar las lesiones típicas, como las nucleares y la producción de osteoide.11
El tratamiento dependerá del estadio en el que se encuentre el paciente, del presupuesto y de los tiempos de supervivencia, todo esto logrando un protocolo funcional adecuado a cada paciente.11
El uso de analgésicos es necesario para controlar de forma efectiva y adecuada el dolor nociceptivo desde el primer indicio de la signología clínica hasta la terapia definitiva. Así, se recomienda un plan analgésico multimodal que incluya el uso de AINE, como carprofeno o firocoxib, y el uso de derivados opiáceos, como tramadol.11
La cirugía, como la amputación o la cirugía con preservación, es el método de elección para el tratamiento del osteosarcoma. El principal objetivo es la resección del tumor primario para controlar y mitigar el dolor y, al mismo tiempo, limitar el proceso de metástasis al frenar la proliferación de células y su diseminación hacia otras zonas anatómicas y tejidos.11
Posterior al tratamiento quirúrgico, la principal causa de mortalidad poscirugía es el desarrollo de metástasis. La utilización de medicamentos citotóxicos, como la quimioterapia, prolonga el periodo de supervivencia posquirúrgica. Los fármacos más utilizados para el tratamiento del osteosarcoma son cisplatino, carboplatino y doxorrubicina. Los tiempos de supervivencia reportados en pequeñas especies son de entre 104 y 413 días, aproximadamente.11
Presentación del caso
Se presenta el día 30 de julio de 2025 a nuestras instalaciones un ejemplar macho de iguana verde (Iguana iguana) adoptada en enero 2025 sin historia del tutor anterior. Se observó un crecimiento anormal, con cambio de color, en el miembro pélvico izquierdo, con algesia en el miembro y disminución de su consumo de alimento. Originalmente, se alimentaba de espinaca, tulipanes silvestres, mango, plátano, uva y fresa. Se mantenía con exposición al sol y de libre acceso en el domicilio.
Historia clínica
Se realiza un examen físico general en el que se observa un aumento de tejido en la región distal de las falanges del miembro pélvico derecho de coloración negro a rojizo, bien delimitado, ulcerativo, con presencia de líquido seropurulento; con baja condición corporal 2/5, presencia de lesiones sugerentes de estomatitis, porcentaje de deshidratación del 6%, hiporexia, con 23.4°C de temperatura corporal, con algesia a la locomoción y agresividad (fig. 1).

Pruebas complementarias
Se realizó una punción con aspiración de aguja fina de la lesión, se realizó un extendido en un portaobjetos de 1” × 3” y se mandó a su análisis en el laboratorio de diagnóstico.13
Se realizó una venopunción en la vena caudal en la zona ventral de la cola con jeringa de 3 mL con aguja de 23G y se colocó en un tubo de heparina para su procesamiento.13
Se tomaron proyecciones ventrodorsal y dorsoventral del miembro pélvico y de la cavidad celómica; asimismo, se tomaron proyecciones laterolaterales izquierda y derecha de la cavidad celómica para observar la estructura ósea y, en caso de que fuera positivo, metástasis.11,12
Diagnóstico y discusión
En la citología se reportó material citológico representado por un fondo ligeramente basófilo y granular, abundantes neutrófilos con cambios degenerativos moderados, macrófagos espumosos, así como células redondeadas poco delimitadas con escasas vacuolas citoplasmáticas; otras tenían un citoplasma claro, con núcleo único redondeado y patrón de cromática fino-granular; también se reportaron linfocitos maduros y sin atipias. Por lo anterior, el diagnóstico reportado fue de inflamación piogranulomatosa séptica y de tumor de células redondas. La recomendación de patología fue realizar un estudio histopatológico.
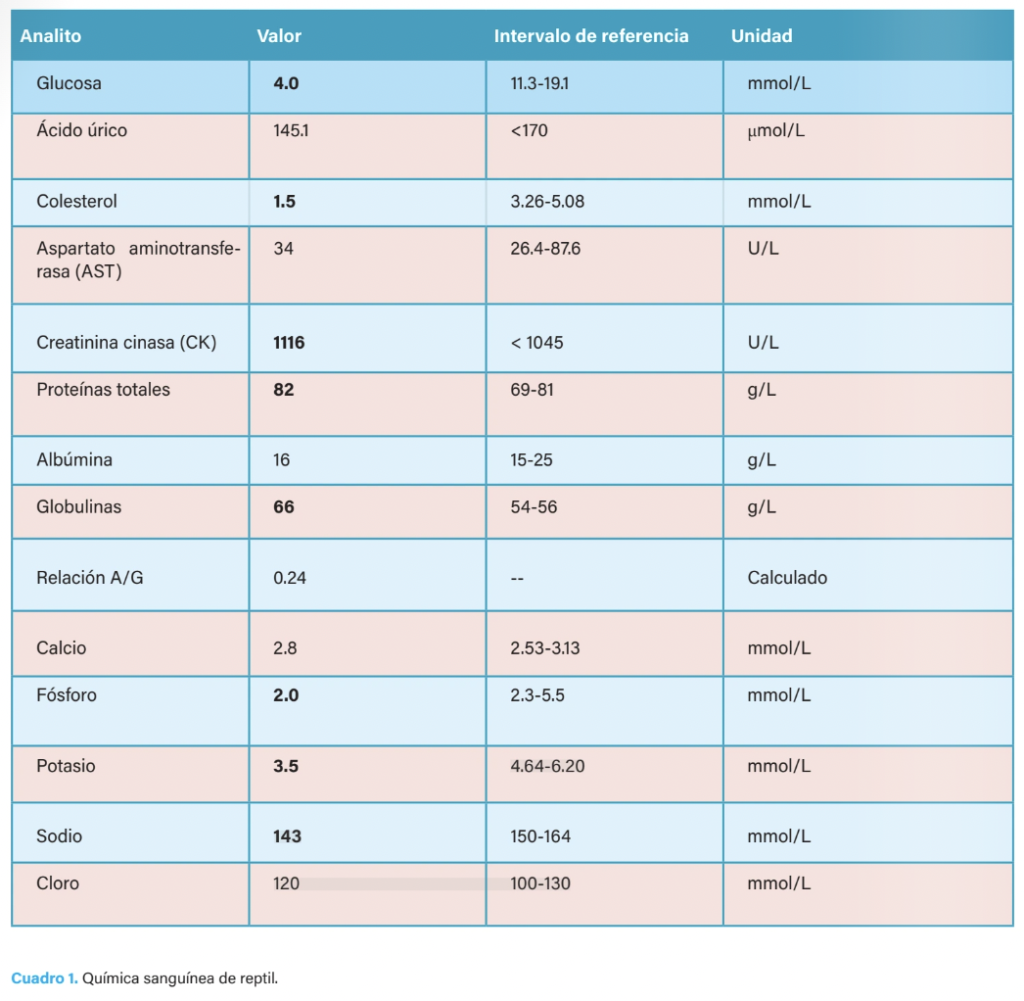
En la bioquímica sanguínea se reportaron hipocolesterolemia, hipofosfatemia, hipocalemia e hiponatremia derivadas de un bajo aporte nutricional, así como hiperproteinemia por hiperglobulinemia, relacionada con la estimulación antigénica y la inflamación (cuadro 1).
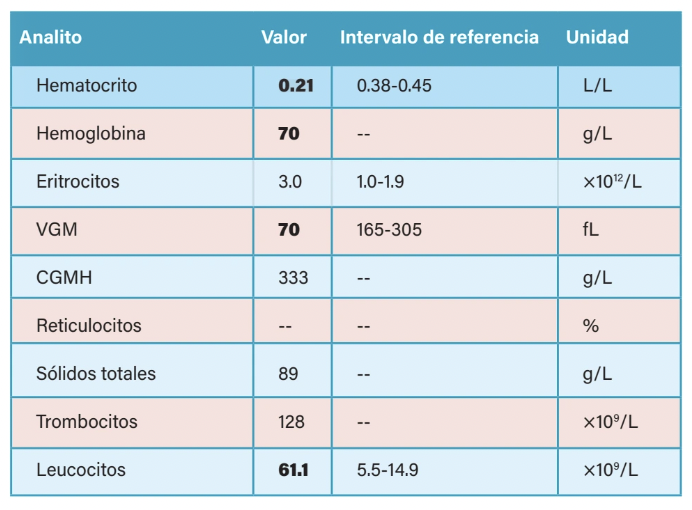
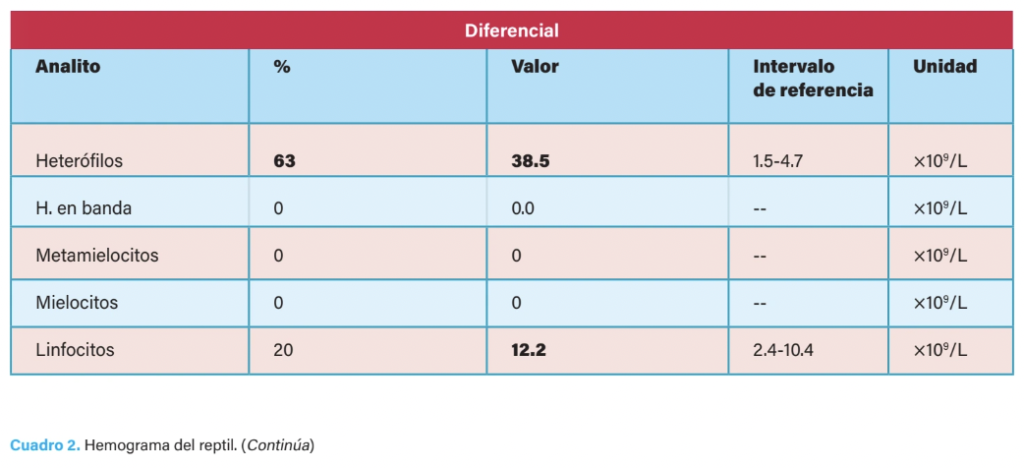
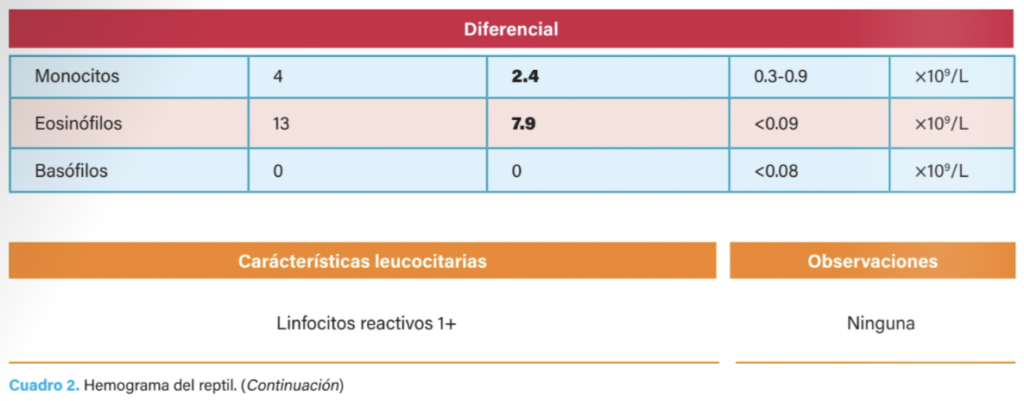
Por su parte, en el hemograma se reportaron anemia relacionada con enfermedad inflamatoria, leucocitosis por neutrofilia y monocitosis relacionadas con inflamación crónica, linfocitosis relacionada con estimulación antigénica inespecífica y eosinofilia asociada con degradación de proteínas en tejidos (cuadro 2).

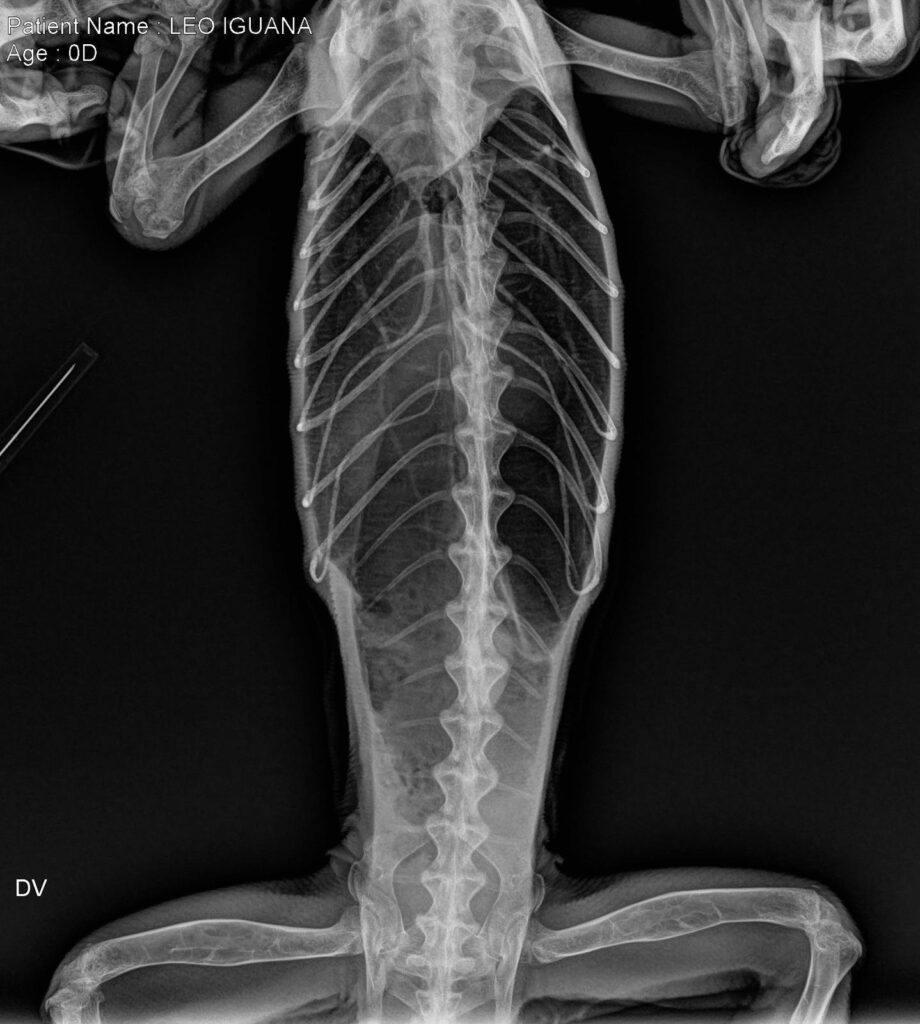
En la placa radiográfica de la cavidad celómica no se observaron estructuras sugerentes de metástasis ni daño en la estructura ósea de la columna vertebral (figs. 2 a 4).
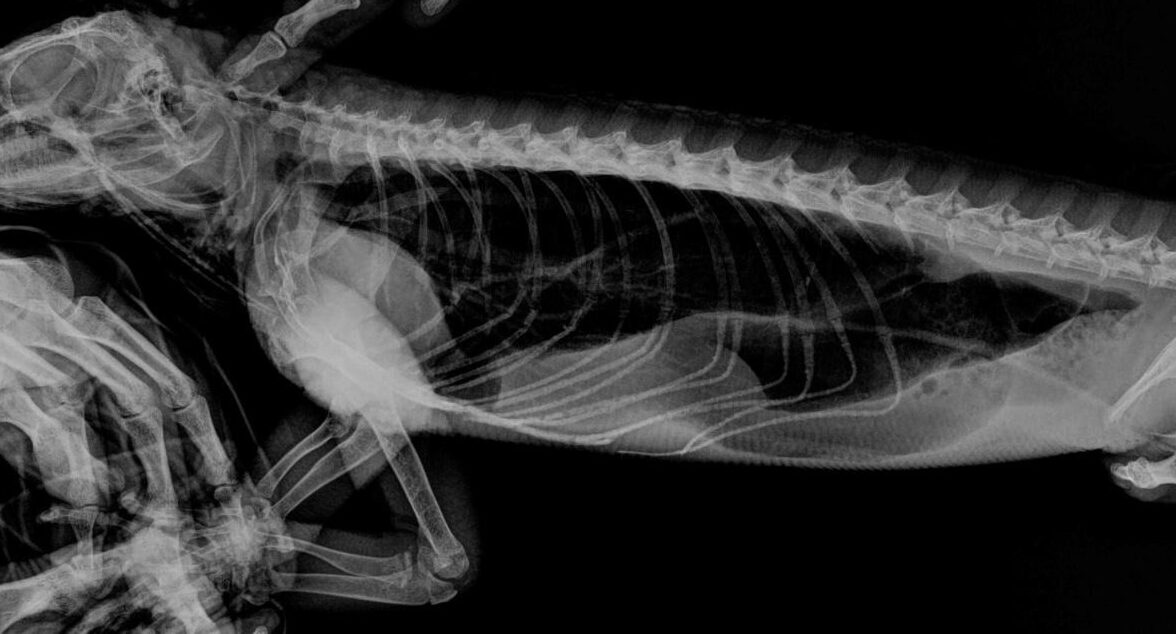
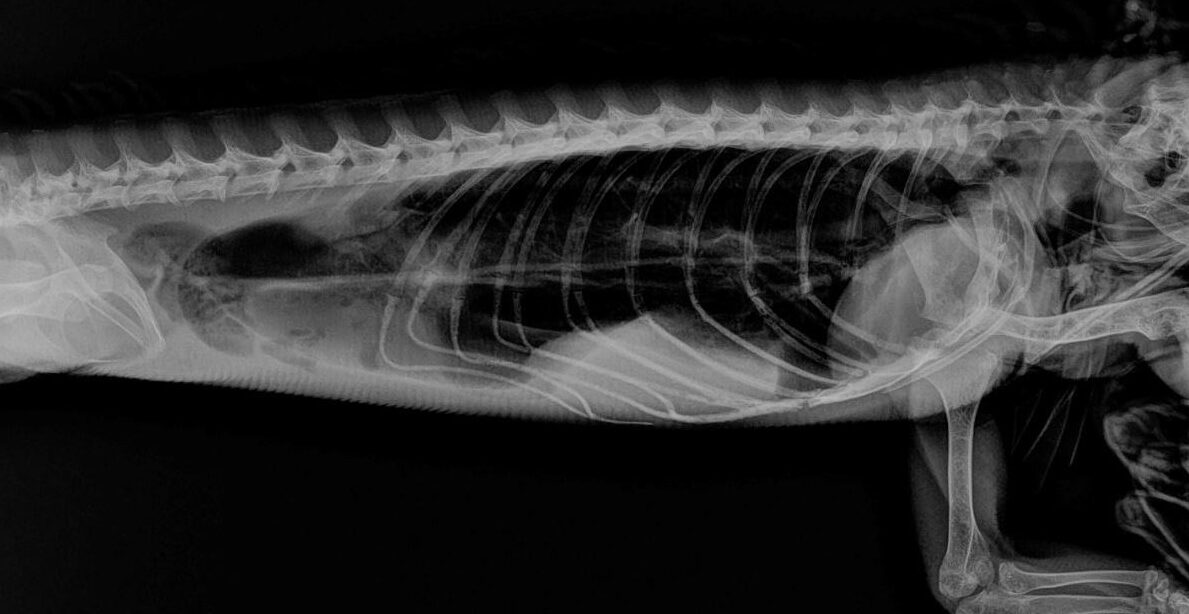
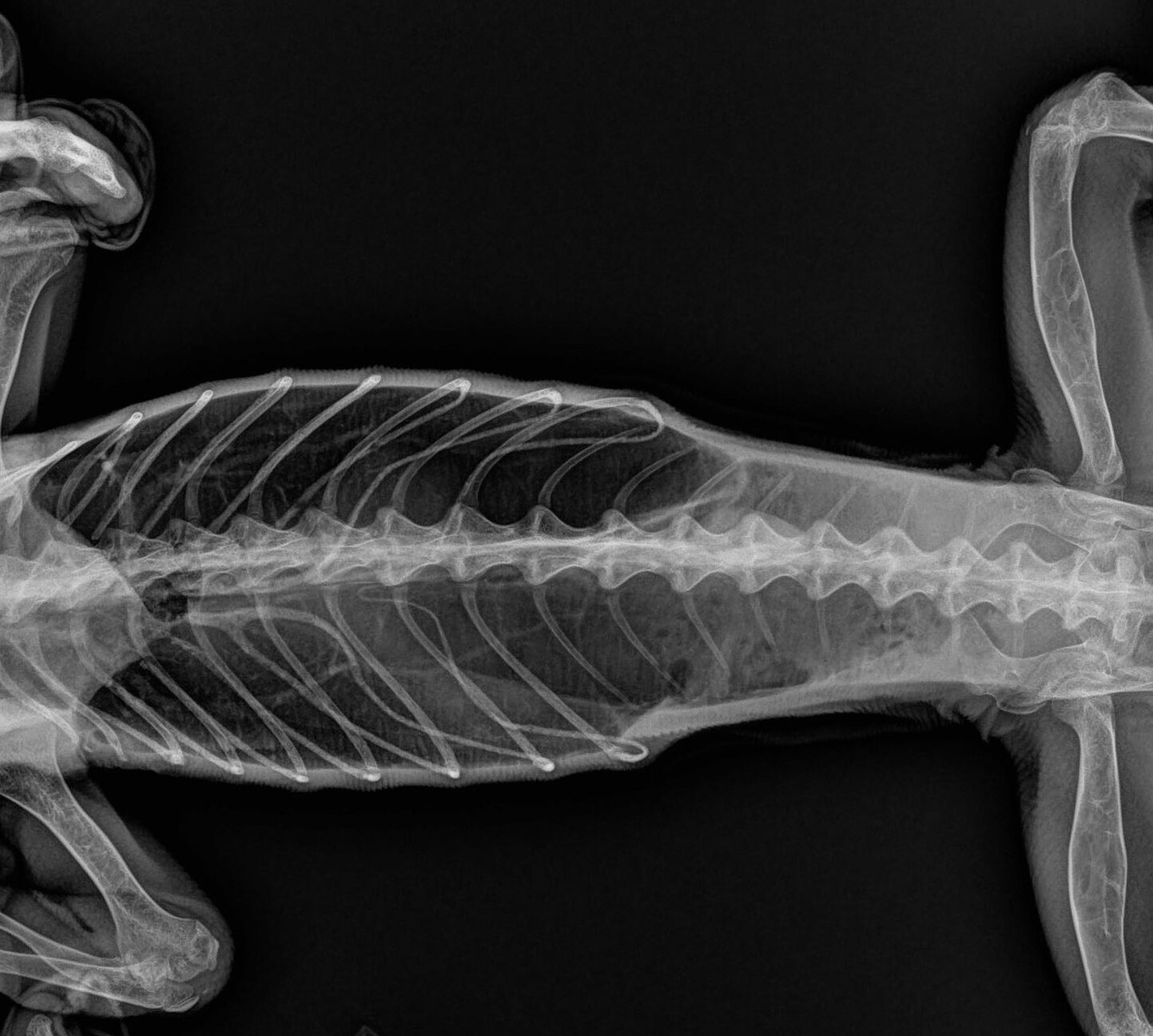
En la placa del miembro afectado se observó una masa que involucraba la tercera falange, con estallamiento y degradación del tercer metatarso, que ya implicaba al segundo metatarso y con pérdida de estructura y densidad óseas (fig. 5).
Tratamiento
Se planteó la resección quirúrgica con amputación del miembro hasta la articulación tarsometatarsiana izquierda. Se administró atropina de 0.04 mg/kg por vía IM en preanestesia y, como protocolo anestésico general, la combinación de ketamina 30 mg/kg con xilazina 1 mg/kg IM, con un periodo de 45 a 60 minutos de anestesia continua, además de infiltración de lidocaína al 2% en la articulación tarsometatarsiana.
Se realizó un corte directo en la articulación con bisturí de núm. 4 y con ligadura del paquete vascular con nudo de cirujano, diseccionando el músculo y el paquete neurovascular para evitar complicaciones hemorrágicas y de percepción nociceptiva.
Se retiró toda la lesión sin complicaciones quirúrgicas y se realizó una sutura con ácido poliglicólico de 2-0 en forma de jareta o sutura en forma de bolsa de tabaco sin colocación de dren y con vendaje de compresión para amputación15 (figs. 6 y 7).
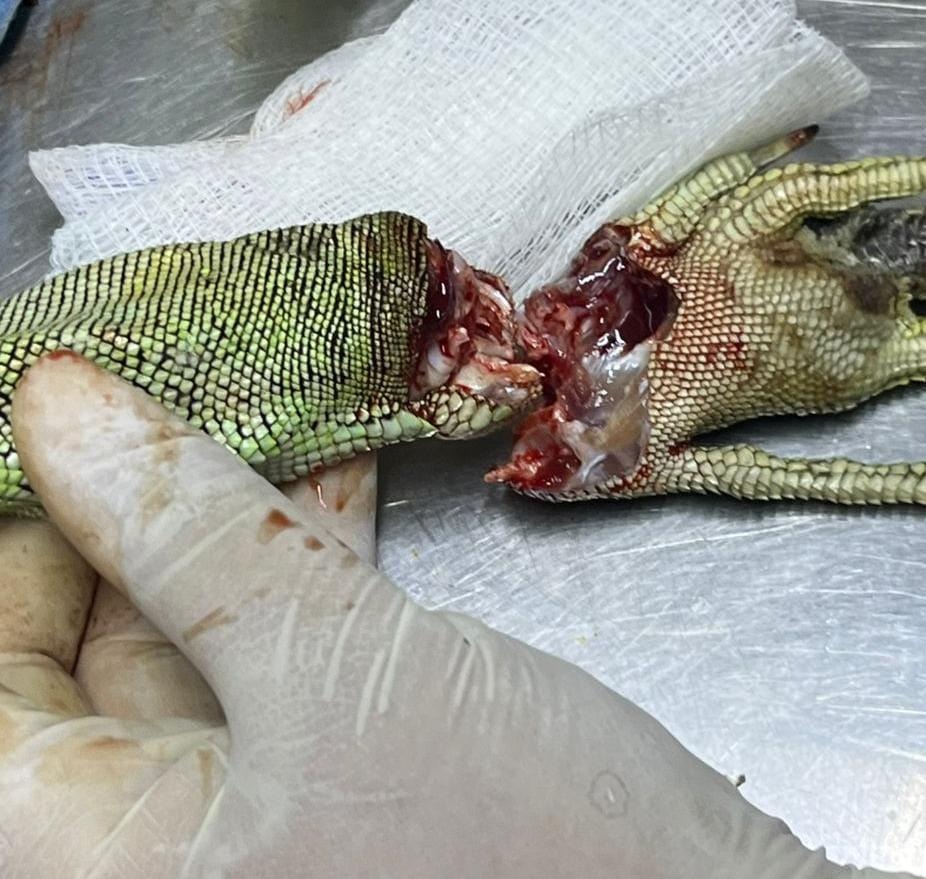
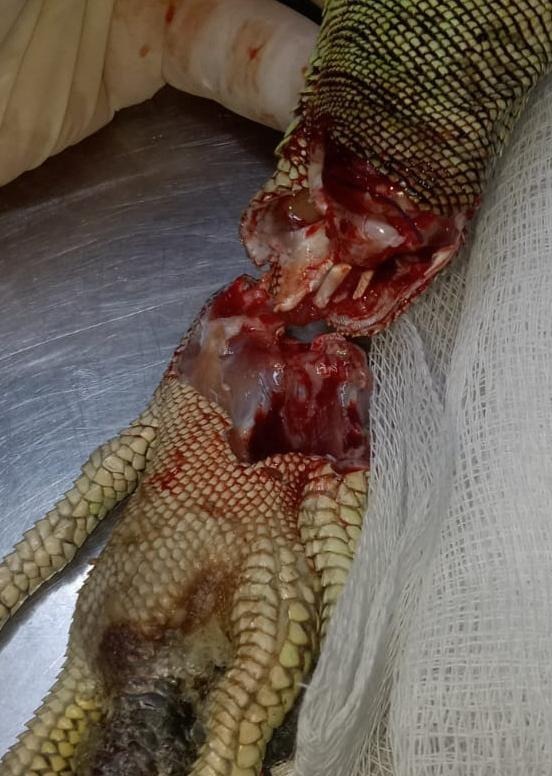
Se le administró enrofloxacina a dosis de 5 mg/kg por vía IM, junto con tramadol a dosis de 10 mg/kg por 5 días, una vez al día, junto con cambio de alimentación.14
Conclusiones y resultados
El diagnóstico morfológico final de la lesión analizada fue de un osteosarcoma condroblástico con metástasis a piel, tejido adiposo y músculo esquelético, la cual fue resecada en su totalidad.
El ejemplar no continuó con el tratamiento quimioterapéutico por respuesta de su tutor. A la evaluación posquirúrgica a los 25 días, se notaba de mejor ánimo, con un aumento de alrededor de 350 gramos y un apetito más evidente, sin signos de dolor.
En este sentido, las neoplasias de origen musculoesquelético en las iguanas representan el 6% de las neoplasias. El abordaje con cada paciente debe realizarse siguiendo lineamientos encaminados a dar una resolución clínica sustentada en evidencia clínica para favorecer la calidad de vida de los pacientes.
Referencias
- Brown J, Amend S, Austin R, Gatenby R, Hammarlund E, Pienta K. Updating the Definition of Cancer. Pubmed central 2023 21(11):1142-1147.
- De la Garza J, Juárez P. Antecedentes. En: De la Garza J, Juárez P (eds.). El cáncer. México: Editorial Universidad Autónoma de Nuevo León, 2014;21-33.
- De la Garza J, Juárez P. ¿Qué sabemos del cáncer en el momento actual? En: De la Garza J, Juárez P (eds.). El Cáncer. México: Editorial Universidad Autónoma de Nuevo León, 2014;34-35.
- Gersten T, Biblioteca Nacional de Medicina. Tumor óseo. Medline Plus, Enciclopedia médica. Disponible en: medlineplus.gov/spanish/ency/article/001230.htm
- American Academy of Orthopedic Surgeons, Diseases & Conditions. Bone Tumor. Disponible en: orthoinfo.aaos.org/en/diseases—conditions/bone—tumor/
- American Academy of Orthopedic Surgeons, Diseases & Conditions. Metastasic Bone Disease. Disponible en: orthoinfo.aaos.org/en/diseases—conditions/metastasic-bone-disease/
- Boston S. Musculoskeletal neoplasia and Limp-Sparing Surgery. En: Tobias KM, Spencer AJ (eds.). Veterinary Surgery: Small Animal. St Louis, Missouri: Elsevier, 2012;117-1159.
- Ehrhart NP, Stewart DR, Fan TM, Tumors of the skeletal system. En: Withrow & Mac Ewen’s Small Animal Clinical Oncology. St Louis Missouri: Elsevier, 2014;464-495.
- Kirpenjesteijn J, Kik M, Rutterman GR, Teske E. Prognostic signifficance of a new histologic grading system for canine osteosarcoma. Vet Pathol 2002;39(2):240-6
- Schmidt AF. Nielen M, Klungel OH, Hoes AW, De Boer A, Groenwold RH, Kirpenjesteijn J. Prognostic factors of early metastasis and mortality in dogs with apendicular osteosarcoma after receiving surgery: an individual patient data meta-analysis. Prev Vet Med 2013;112 (3-4):414-22.
- Belda B, Lara A, Lafuente P. Osteosarcoma apendicular canino: ¿Qué opciones tenemos? Clin Vet Peq Anim 2016;36(4):241-255.
- Thrall DE. Radiographic features of bone tumors and bone infections. En: Thrall DE (ed.). Textbook of Veterinary Diagnostic Radiology. St Louis Missouri: Elsevier 2013;307-317.
- Divers SJ. Procedimientos clínicos para reptiles. University of Georgia, Department of Small Animal Medicine and Surgery, 2020. Disponible en: msdvetmanual.com/es/animales-exóticos-y-de-laboratorio/reptiles/procedimientos-clínicos-para-reptiles
- Carpenter JW. Reptiles. En: Marion CJ, Carpenter JW (eds.). Exotic Animal Formulary. St Louis Missouri: Elsevier, 2018;127-163.
- Heard D, Fleming G, Lock B, Jacobson E. Saurios. En: Meredith A, Redrobe S. Manual of Exotic Pets, Fourth Edition. Gloucester, Inglaterra: British Small Animal Veterinary Association (BSAVA), 2012;317-342.

Leave a reply