
Implementación de los marcadores genéticos BRCA1 y BRCA2 como herramienta diagnóstica de cáncer de mama hereditario: reporte de un caso
AUTOR: MVZ Dipl. Brenda Gómez
Resumen
El cáncer de mama es uno de los tumores más comunes en perras adultas no esterilizadas, por lo que se han buscado herramientas que faciliten el diagnóstico oportuno. En este artículo se presenta un caso clínico de un paciente de cáncer de mama con diagnóstico histopatológico y molecular por medio de marcadores genéticos BRCA1 y BRCA2.
Palabras clave: BRCA1, BRCA2, cáncer mamario canino, reacción en cadena de la polimerasa (PCR)
Abstract
Breast cancer is one of the most common tumors in unspayed adult dogs, and tools are being developed to allow a timely diagnosis. This article presents a clinical case of a dog with breast cancer, focusing on the histopathological and molecular diagnosis using the BRCA1 and BRCA2 genetic markers.
Keywords: BRCA1, BRCA2, canine mammary cancer, polymerase chain reaction (PCR)
Introducción
El cáncer de mama es uno de los tumores más comunes en perras adultas no esterilizadas.1 Se han contemplado como factores de riesgo para su aparición, desarrollo y progresión la edad, la nutrición, el sexo y el estado reproductivo. En ciertas razas se observa una alta susceptibilidad al cáncer mamario canino, lo que sugiere un componente hereditario importante.2,3 Diversas investigaciones han estudiado ciertos marcadores genéticos que se han relacionado con el desarrollo del cáncer de mama tanto en humanos como en animales y de esta forma se busca detectar de manera oportuna este tipo de enfermedades.2 Este es el caso de las variantes de los genes de BRCA1 y BRCA2, los cuales tienen un papel significativo en el desarrollo del cáncer de mama y ovario hereditario.3
Función y estructura de los genes BRCA1 y BRCA2
Los genes BRCA1 y BRCA2 se encuentran en los cromosomas 9 (fig. 1) y 25 (fig. 2), respectivamente, y pertenecen a la familia de genes de reparación del ADN. Desempeñan una función reguladora en el ciclo celular, al codificar proteínas involucradas en la reparación del daño al ADN y al funcionar como genes supresores de tumores; es decir, interactúan y participan en la síntesis de complejos multiproteicos (fig. 3) que garantizan la regulación transcripcional y postranscripcional, el reconocimiento y la corrección de roturas de la doble cadena.3
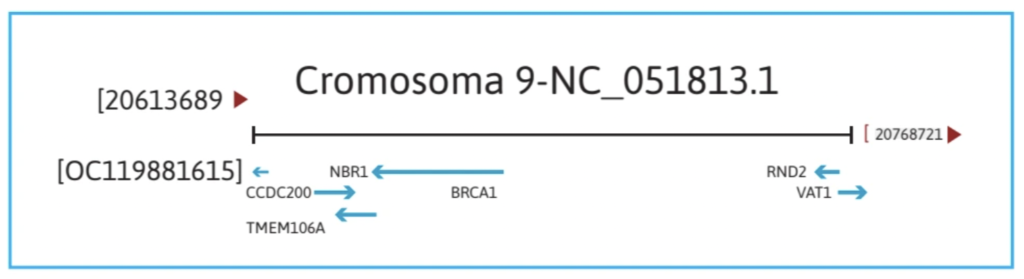
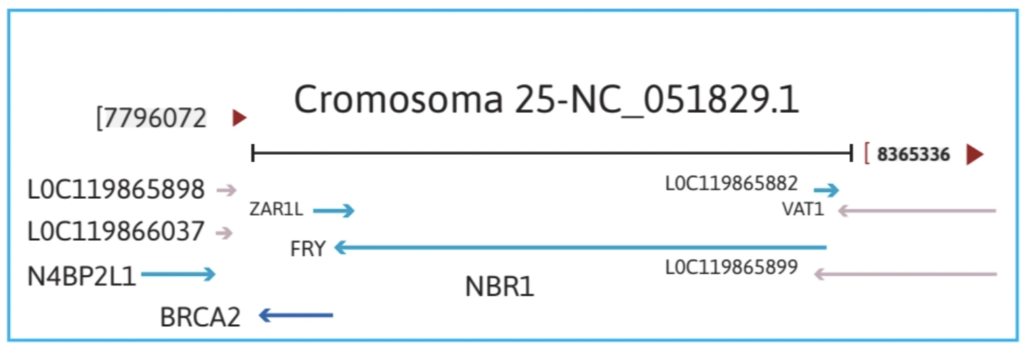
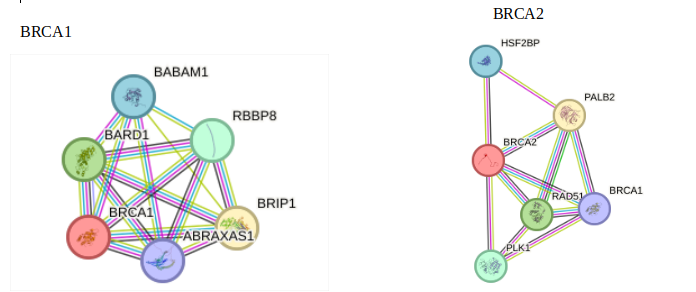
Los genes BRCA1 y 2 interactúan con otros genes, participando en la síntesis de complejos multiproteicos que regulan la transcripción y la corrección de roturas de doble cadena. Los genes BRCA1 y BRCA2 se encuentran presentes en perros de manera natural; sin embargo, una variación en estos genes puede provocar una pérdida de su función y, como consecuencia, aumentar la probabilidad de desarrollar cáncer de mama4.
Debido a la alta incidencia de tumores mamarios y a la agresividad con que suelen manifestarse,1 se han buscado alternativas para la detección oportuna de esta enfermedad. En el presente trabajo se amplificaron las variantes genéticas de BRCA1 y BRCA2 relacionadas con el cáncer de mama en un caso clínico, con el objetivo de presentar una alternativa útil y precisa para el diagnóstico de cáncer de mama en perros.
Caso clínico
Luna, canino, mestizo, hembra no esterilizada (fig. 4); al momento de manifestar la enfermedad tenía 8 años de edad. Se presentó a consulta por dos masas en la glándula mamaria inguinal (una del lado derecho y otra del lado izquierdo) de aproximadamente 3 mm × 2 mm × 3 mm. En consecuencia, se decidió realizar la prueba de reacción en cadena de la polimerasa (PCR) para la detección de variantes en los genes BRCA1 y BRCA2. A la par, se realizó cirugía (nodulectomía de ambos tumores) para el retiro de las masas y se enviaron a análisis histopatológico.

Materiales y métodos
Método de histopatología
Se obtuvo una muestra de tejido tumoral completo y se preservó en formol al 10% para su procesamiento. Se envió al citotecnólogo para manejo, tinción y corte del tejido tumoral y posteriormente se envió al área de patología para su análisis.
Análisis molecular
Se obtuvo una muestra de sangre total, la cual fue colectada de sangre periférica (vena cefálica) y preservada en tubos con EDTA para su procesamiento posterior. Para la extracción de ácidos nucleicos, se realizó mediante el kit de extracción Quick- DNATM Miniprep Plus kit, números de catálogo D4068 & D4069, siguiendo las instrucciones del fabricante.
Para la elaboración de la reacción en cadena de la polimerasa (PCR) se utilizó el termociclador MiniPCR, con los primers tomados de las secuencias de referencia del NCBI: NC_051829.1 Reference ROS_Cfam_1.0 y NC_051813.1 Reference ROS_Cfam_1.0.
De acuerdo con las especificaciones del Manual de usos y procedimientos de laboratorio Oncogenes CDMX®, se utilizó 6 ng/μL de ADN, 10 uM de primers, 2 mM de dNTP, 5 U/μL de Taq Pol, 10× de buffer, 30 mM de MgCl y 100× de BSA.
La PCR se lleva a cabo en un volumen final de 20 μL, empleando las siguientes condiciones: un ciclo de desnaturalización inicial a 94°C/3’, 30 ciclos de desnaturalización a 94°C/30”, alineación en gradientes/30” y extensión a 72°C y un ciclo de extensión final a 72°C/3’. Se realizó con un gradiente de temperatura de disociación (TM) de 66.7-67.8°C.
Posteriormente, se utilizó electroforesis para la observación de los resultados, para lo cual se empleó un gel de agarosa al 2% y se le adicionó 1 μL del colorante ViSAfe Green gel. Se colocó en la cámara de electroforesis, junto con 30 mL de TBE al 10%. Por último, se cargaron las muestras y se realizó la electroforesis.
Resultados
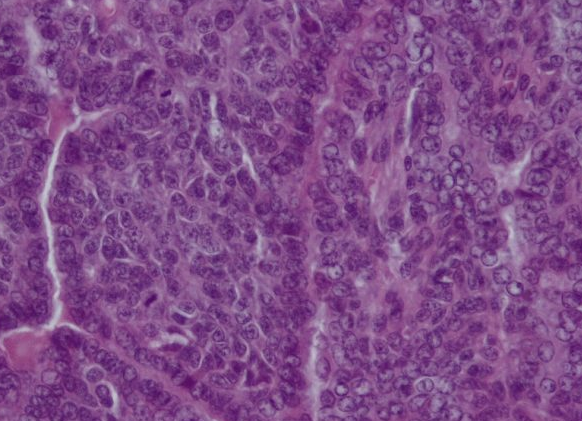
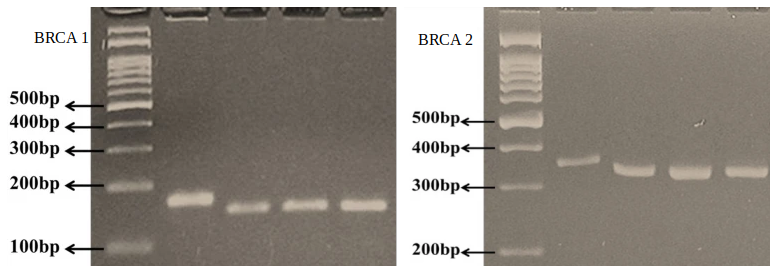
Se realizó el estudio histopatológico de las masas analizadas, obteniendo como resultado “adenocarcinoma de glándula mamaria” (fig. 5). De igual manera, se realizó el estudio de PCR de BRCA1 y BRCA2, en el que se obtuvo un resultado positivo para ambos marcadores (fig. 6), concordando en ambos estudios.
Discusión
Según las referencias de Withrow J. et al. y Torres G. et al., la histopatología puede considerarse una herramienta de gran utilidad para la detección de células cancerosas; sin embargo, la interpretación de los resultados suele depender del operador, es decir, de la experiencia del patólogo o del técnico laboratorista que la interpreta. De igual modo, depende de la región de la lesión en la que se haya realizado el corte histológico que se está analizando. Por otro lado, el presente estudio, así como Panagopouloula M, concuerdan en que la evaluación de las variantes BRCA1/2 puede ser una herramienta de alta precisión, debido a su repetibilidad estadística, para la detección de cáncer de mama. Además, ofrece la oportunidad de monitorear a los pacientes que presentan la variante antes de desarrollar la enfermedad, a diferencia de la biopsia, que se realiza una vez que la enfermedad ya se ha manifestado.
Conclusiones
El cáncer es una enfermedad de origen genético, por lo que el uso de herramientas moleculares, como la PCR, para la detección de genes asociados a tumores, como en este caso, resulta útil y poco invasivo, ya que no requiere anestesia para obtener la muestra a analizar. Además, al no ser una prueba que depende de la experiencia de los médicos, técnicos de laboratorio o patólogos para su análisis, se vuelve una herramienta de alta precisión a costos cada vez más accesibles.
Lo mismo ocurre en el caso de los marcadores BRCA1 y BRCA2; es decir, se puede realizar la detección oportuna al identificar las variaciones asociadas al cáncer de mama hereditario antes de que se manifieste la enfermedad, lo que podría ayudar a iniciar un tratamiento temprano o, en el mejor de los casos, preventivo.
Referencias
- Withrow SJ, Vail DM, Thamm DH, Liptak JM (eds.). Oncología clínica de pequeños animales. España: Editorial Edra, 2022:455.
- Thumser-Henner P, Nytko KJ, Rohrer-Bley C. Mutations of BRCA2 in canine mammary tumors and their targeting potential in clinical therapy. BMC Veterinary Research 2020;16(1):30.
- Enginler SO, Akış I, Toydemir TSF, Oztabak K, Haktanir D, Gündüz M et al. Genetic variations of BRCA1 and BRCA2 genes in dogs with mammary tumours. Vet Res Commun 2014;(38):21–27.
- Zeng L, Wei L, Chen CS. Breast cancer animal models and applications. ZR Zoological Research 2020;41(5):477–494.
- Varol U, Kucukzeybek Y, Alacacioglu A, Somali I, Altun Z, Aktas S. BRCA1 and BRCA2 genes. Medical Oncology Clinic 2018;23(4):862-866.
- Torres G, Eslava PR. Tumores mamarios en caninos: adenocarcinoma complejo de glándula mamaria con metástasis a ganglio linfático regional. Orinoquia 2007;11(1):99-110.
- Panagopoulou M, Theodoros P, Anastasios G. BRCA1 & BRCA2 methylation as a prognostic and predictive biomarker in cancer: Implementation in liquid biopsy in the era of precision medicine. Clinical Epigenetics 2024;16(178):2-16.

Leave a reply